- SURFACE (TRAITEMENTS DE)
- SURFACE (TRAITEMENTS DE)On entend par «traitements de surface» toutes les opérations mécaniques, chimiques, électrochimiques ou physiques qui ont pour conséquence de modifier l’aspect ou la structure de la surface des matériaux, afin de l’adapter à des conditions d’utilisation données.Le but des traitements de surface est fort variable: ils peuvent tendre à améliorer les propriétés optiques (ou l’aspect esthétique), la résistance à la corrosion sèche ou humide, la tenue de surfaces soudées, la conductivité, les propriétés mécaniques, la résistance au frottement et à l’usure.Le nombre et la disparité des traitements de surface sont pratiquement infinis. Cependant, l’élaboration d’un traitement donné, son comportement dans les conditions d’utilisation, son efficacité, sa durée de vie peuvent être en bonne partie décrits et prévus par la connaissance de quelques principes de base gouvernant les phénomènes fondamentaux que sont la corrosion électrochimique ou la corrosion sèche, la diffusion à l’état solide, la plasticité.C’est en partant de ces notions qu’il est possible d’envisager une étude rationnelle des traitements de surface.1. Traitements de surface et électrochimieLe but principal des traitements de surface par voie électrochimique est de protéger les métaux ou alliages contre la corrosion qui correspond à la dissolution du métal; c’est une réaction d’oxydation, donc une réaction anodique ; en conséquence, nous distinguerons les traitements anodiques et cathodiques.Traitements anodiquesOn peut réduire la vitesse de corrosion en augmentant la polarisation anodique. L’exemple typique de ce procédé est la passivation . Il s’agit de former une couche protectrice, en général un oxyde ou un hydroxyde, à la surface du métal.Si le métal considéré est passivable , il est possible d’assurer sa protection en accroissant son potentiel de dissolution; le but est atteint soit en imposant un potentiel donné, suffisamment élevé pour provoquer la passivation, mais inférieur au potentiel de transpassivité qui correspond à la destruction de la couche protectrice, soit en favorisant les réactions de réduction (dépolarisation des réactions cathodiques). Cette dernière solution est la plus employée; elle peut être obtenue en utilisant des peintures oxydantes (minium) ou en mettant le métal, généralement des aciers doux, en contact avec une solution basique (protection par alcalinisation) qui provoque la création d’une couche passivante formée principalement d’oxyde Fe34. Cette couche est adhérente et protectrice dans les solutions basiques, tandis qu’elle perd ses propriétés dans des solutions acides agressives.Lorsque le métal à protéger est très oxydable, il est intéressant de former par voie électrochimique une couche d’oxyde protectrice; l’oxydation anodique de l’aluminium est l’un des procédés les plus connus pour protéger et décorer les alliages légers. Les solutions utilisées sont à base d’acides sulfurique, chromique ou oxalique. Comme le traitement s’effectue par oxydation directe du métal, l’état de surface initial n’a qu’une faible influence sur l’adhérence des couches formées. Le caractère protecteur des couches est dû à la faible vitesse de diffusion des ions du métal à travers l’oxyde. Bien que l’oxyde présente des pores allongés perpendiculaires à la surface, le métal reste protégé par une barrière d’oxyde de quelques nanomètres d’épaisseur. Ces pores peuvent être obturés par l’hydratation de l’alumine dans l’eau bouillante contenant des sels colorants ou non.L’oxydation anodique du tantale permet de fabriquer des films diélectriques d’environ 300 nm qui servent de condensateurs; mais ce dernier procédé n’est pas réellement un traitement de surface.Un dernier traitement anodique est le polissage électrolytique, qui donne une surface plane exempte de défauts microgéométriques et permet d’éliminer les couches superficielles écrouies par polissage mécanique par exemple. Les conditions et les bains de polissage varient d’un métal à l’autre; il est néanmoins toujours nécessaire de porter le métal à un potentiel tel que le courant anodique soit limité par la diffusion des ions dans la solution.Si le métal à polir est passivable, le potentiel appliqué se trouve obligatoirement dans le domaine de transpassivité.Enfin, signalons le décapage des aciers dans des solutions chlorhydrique ou sulfurique. Ce procédé peut être dangereux dans la mesure où l’hydrogène cathodique formé diffuse dans le métal et provoque une fragilisation. Afin d’éviter ces dangers, un inhibiteur de corrosion est ajouté à la solution; il a pour but de stopper la réaction lorsque le métal est à nu.Traitements cathodiquesÀ toute dissolution du métal en solution correspond une réaction cathodique qui, en général, est une réduction de l’hydrogène ou de l’oxygène dissous. Il convient donc, pour limiter l’intensité du courant de corrosion, d’abaisser le potentiel de dissolution à une valeur inférieure ou égale à celle du potentiel d’équilibre du métal considéré ou d’augmenter la surtension de la réaction cathodique.Un type de protection cathodique, appelé également protection par électrode sacrifiée, consiste à couvrir le métal d’un revêtement anodique; l’exemple classique est celui de la galvanisation du fer. La présence de fissures dans ces revêtements n’est pas dangereuse dans la mesure où le métal sous-jacent joue le rôle de cathode (fig. 1 a).Mais ces revêtements ont pour inconvénient de se détériorer avec le temps. En outre, les réactions cathodiques locales peuvent avoir des conséquences néfastes pour les propriétés mécaniques du métal. L’hydrogène introduit dans les aciers pauvres en carbone provoque en effet une fragilisation d’autant plus importante qu’ils sont sous contrainte.D’autres procédés se fondent sur le ralentissement des réactions cathodiques, soit en diminuant les vitesses de diffusion de l’oxygène (inhibiteur de surface) dans la solution, soit en augmentant la surtension en hydrogène.Dépôts métalliques et minérauxÀ l’exclusion du revêtement par certains métaux précieux, un grand nombre de revêtements métalliques sont effectués par électrolyse: zinc, cadmium, nickel, chrome, cuivre... Le cuivre est en général déposé comme sous-couche avant un autre dépôt électrolytique (Zn, Cr, Ni) dont il améliore l’accrochage. Le but recherché est soit la décoration, soit la protection, soit les deux simultanément; l’épaisseur des couches déposées est en général comprise entre quelques micromètres et quelques centaines de micromètres.Les dépôts par électrolyse sont très employés en raison de leur grande souplesse; on dispose en effet d’un grand nombre de paramètres pour modifier la structure et l’épaisseur des revêtements: composition des bains, densités de courant, tension, temps d’électrolyse, recuits de diffusion, etc. Cependant, dans le cas d’un dépôt de nickel sur le fer, la moindre fissure dans le revêtement se traduit par la formation d’une cellule de corrosion où le fer joue le rôle d’anode et est attaqué à grande vitesse (fig. 1 b); tous les revêtements protecteurs passivés de chrome, d’aluminium, de tantale présentent le même inconvénient dans la mesure où ils sont cathodiques vis-à-vis du métal à protéger.En dehors de l’électrolyse, il est possible de déposer un métal sur un autre par réaction d’échange, à condition que le métal à protéger possède un potentiel de dissolution faible ou négatif; cette propriété est utilisée pour déposer du cuivre sur du fer par exemple.Si l’agent réducteur n’est pas le métal de base mais un agent en solution (anions H2P2-), pour déposer du nickel, le procédé est alors appelé électroless.Au lieu de revêtements métalliques, il est possible de déposer des composés minéraux; la protection des aciers par phosphatation consiste à mettre la surface du métal en contact avec une solution contenant des orthophosphates diacides de fer, de manganèse ou de zinc (phosphatation cristalline) ou des orthophosphates alcalins (phosphatation amorphe). Dans le premier cas, le fer est attaqué par l’acide phosphorique, ce qui entraîne la transformation des orthophosphates en phosphates insolubles; dans le second cas, c’est le phosphate de fer lui-même qui est précipité.L’état de surface a une grande influence sur les réactions électrochimiques; c’est la raison pour laquelle il est nécessaire d’effectuer un dégraissage suivi d’une «activation» de la surface par sablage. La phosphatation assure une protection efficace contre la corrosion et une bonne tenue à l’usure et au frottement.La chromatation est un procédé fondé sur une réaction électrochimique qui provoque la précipitation en couche fine d’un mélange d’hydroxyde de chrome et d’oxyde du métal à protéger. Ce traitement est utilisé pour de nombreux métaux tels que l’aluminium, le cadmium, le zinc, le cuivre, le magnésium, l’argent... Les bains contiennent des chromates en solution plus ou moins acide selon le métal considéré; ils peuvent également contenir des phosphates pour combiner phosphatation et chromatation.Dépôts organiquesLes dépôts organiques sont essentiellement des peintures et des polymères. Un grand nombre de peintures sont fondées sur l’intervention d’un mécanisme électrochimique qui peut être cathodique ou anodique.Les peintures cathodiques sont constituées d’un support organique (huiles diverses) et d’un pigment métallique, tel que le zinc, qui se trouve en contact avec le métal à protéger. En outre, l’attaque anodique du zinc entraîne la formation de composés solides qui bouchent les pores de la peinture et renforcent son caractère de protection purement physique. Les peintures à caractère anodique utilisées pour protéger le fer et les aciers sont constituées d’oxydes de zinc ou de plomb et d’huile de lin par exemple; il se forme alors des savons qui s’oxydent et favorisent ainsi la passivation du métal. Ces peintures ne servent que de sous-couches, car elles sont perméables; c’est pourquoi il faut les protéger par des peintures de finition qui, outre leur qualité esthétique, sont imperméables à l’eau et aux gaz.Les polymères (polythène, Rilsan, Téflon) ont pris un grand développement; la pièce à protéger est par exemple préchauffée aux environs de 200 0C, puis saupoudrée de polymère. Ces revêtements présentent l’avantage d’une grande diversité d’emploi alliée à des conditions de dépôt souples et faciles.Inhibiteurs de corrosionLes inhibiteurs de corrosion créent une barrière entre le métal et la solution. Ils peuvent provoquer la formation d’un composé insoluble à la surface du métal; ainsi, dans le cas du fer, le bicarbonate de calcium forme du carbonate de fer sur les zones anodiques et de l’hydroxyde de calcium sur les zones cathodiques.Les inhibiteurs organiques (amines grasses, amido-amines, mercaptans...) agissent par adsorption physique en formant une couche monomoléculaire à la surface du métal à protéger qui peut être cathodique, anodique ou mixte.2. Traitements de surface et diffusionL’une des principales qualités d’un dépôt protecteur est son adhérence. Lorsque le traitement de surface est effectué à la température ambiante, il est difficile de préciser la nature exacte, chimique ou physico-chimique, des liaisons entre le dépôt et le métal sous-jacent. L’adhérence d’un dépôt électrolytique par exemple dépend d’un grand nombre de facteurs mal contrôlés: «réactivité» de la surface de départ, contamination éventuelle de cette surface par l’atmosphère, réactions électrochimiques complexes superposées à la réaction de dépôt.Par contre, pour les traitements de surface effectués à température élevée, la zone d’accolement entre le dépôt et le métal de base est soumise aux phénomènes de diffusion à l’état solide, dont les lois sont bien connues et les résultats plus facilement prévisibles. Nous distinguerons trois cas suivant que les phénomènes de diffusion dans le métal à protéger se produisent à partir d’un milieu gazeux, liquide ou solide.Réactions solide-gazLes traitements de surface par diffusion à température élevée à partir d’une réaction entre le métal et un milieu gazeux sont souvent désignés sous le nom générique de «cémentation». Le plus connu est la cémentation proprement dite, c’est-à-dire la carburation superficielle. On doit également classer dans cette catégorie tous les traitements thermiques en atmosphère contrôlée destinés à apporter à la surface des propriétés de protection mécanique ou électrochimique, comme la carbonitruration (chargement superficiel en carbone et en azote), ou certaines métallisations.La succession des réactions se produisant à l’interface gaz-solide est toujours la suivante: décomposition du composé gazeux au voisinage de la surface; formation d’un ou de plusieurs composés ou d’une solution solide entre le métal de base et les éléments d’apport; diffusion en solution solide du ou des éléments d’apport dans les zones proches de la surface; enfin, le composé gazeux est souvent régénéré par des réactions secondaires.Dans le cas de la carburation , l’atmosphère est constituée d’oxydes de carbone CO et C2 ou d’un hydrocarbure tels que le méthane et le propane. Les gaz sont soit introduits directement dans l’atmosphère de recuit, comme pour les hydrocarbures, soit obtenus par décomposition d’un mélange de carbonate et de graphite:
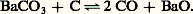 Les oxydes ou les hydrocarbures se décomposent à la surface de l’acier pour donner en particulier du carbone qui forme un carbure superficiel (cémentite), puis pénètre dans le métal par diffusion suivant les deux réactions:
Les oxydes ou les hydrocarbures se décomposent à la surface de l’acier pour donner en particulier du carbone qui forme un carbure superficiel (cémentite), puis pénètre dans le métal par diffusion suivant les deux réactions: En présence de graphite, le gaz carbonique est régénéré par la réaction:
En présence de graphite, le gaz carbonique est régénéré par la réaction: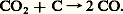 Le choix de la température de cémentation (850 à 1 000 0C) est lié à la grande solubilité du carbone dans l’austénite (2 p. 100 en poids), ce qui revient à dire que le couple de diffusion C/Fe 塚 devient une succession de couches C/Fe3C/austénite et que la forte solubilité du carbone dans l’austénite facilite la réaction de dissociation de la cémentite Fe3C à son interface avec l’austénite. La couche de cémentite est très mince, car la vitesse de diffusion du carbone y est très faible. Cette couche est généralement éliminée par un traitement postérieur dit «de diffusion». Par contre, la couche d’austénite chargée en carbone est épaisse (quelques millimètres). L’acier est ensuite trempé, ce qui transforme la couche cémentée en martensite de haute résistance mécanique. Les traitements de carburation en phase gazeuse sont appliqués pour la protection des métaux réfractaires oxydables (tungstène, molybdène) par une couche très dure de carbure.L’adjonction d’ammoniac à l’atmosphère de traitement, soit seul, soit en même temps que les composés carburants, constitue le procédé de nitruration ou de carbonitruration des aciers. Il se forme en surface une couche mince de nitrure Fe2N, recouvrant une zone profonde où le nitrure Fe4N est réparti en aiguilles dans la structure de l’acier. Ces couches améliorent dans de grandes proportions les propriétés mécaniques de surface des aciers et leur résistance à la corrosion.Les procédés de métallisation en atmosphères oxydoréductrices halogénées à l’équilibre (procédé Galmiche-O.N.E.R.A.) sont fondés sur le transport en phase vapeur de l’élément à déposer, à condition que celui-ci soit plus électropositif que le métal à protéger. En outre, il est nécessaire que les deux métaux possèdent un domaine de solubilité mutuelle à l’état solide. Il est ainsi possible de déposer du chrome sur le fer ou du fer sur le nickel, mais pas l’inverse. Le dépôt est obtenu en plaçant les pièces dans une enceinte sous pression d’hydrogène qui contient en outre une réserve d’halogénure métallique (fluorure, chlorure, etc.) volatil et les métaux d’apport sous forme finement divisée, associés éventuellement avec des constituants auxiliaires tels que des oxydes réfractaires. L’ensemble est porté à une température comprise entre 850 et 1 150 0C.Les équilibres d’oxydoréduction dans l’enceinte aboutissent à un transfert, par l’intermédiaire des halogénures volatils, du métal d’apport entre la poudre et la surface des pièces.Parmi les applications de ce procédé, une des plus répandues est la chromisation des aciers ou des matériaux réfractaires (à base de nickel, de cobalt, de molybdène, de tungstène). Dans le cas du fer ou des aciers par exemple, le traitement effectué à 950 0C environ (c’est-à-dire en phase 塚) aboutit à la formation en surface d’une couche de ferrite chargée en chrome (plus de 13 p. 100 de chrome), comme le montre le diagramme d’équilibre (fig. 2 a). Les grandes vitesses de diffusion du chrome en phase 見 à ces températures provoquent une croissance rapide de cette couche. Par contre, le chrome diffuse très lentement dans l’austénite sous-jacente qui est donc très peu modifiée (fig. 2 b). Après traitement, la surface est par conséquent recouverte d’une couche de quelques dizaines de micromètres d’acier riche en chrome, très résistante à la corrosion puisque passivable dans tous les milieux (fig. 3).Si l’acier a été au préalable carburé, le gainage correspond à une dispersion de carbure de chrome dans une matrice fer-chrome. L’épaisseur est plus faible en raison du blocage de la diffusion du chrome par une barrière de carbures. Par contre, la dureté superficielle est très élevée.Le traitement des superalliages réfractaires par ce procédé, en particulier en vue de leur application dans l’industrie aéronautique (turbines à gaz), met en œuvre un dépôt à partir d’un cément de poudres préalliées de chrome-aluminium («chromaluminisation»). Dans certains cas, les pièces sont prégainées par dépôt électrolytique de nickel ou de cobalt, ou par diffusion à partir d’un cément ternaire Ni-Cr-Ta («tancralisation»).Réactions solide-liquideUn autre type de traitement à température élevée consiste à mettre le métal en présence d’un milieu liquide qui peut être soit un métal en fusion (dépôts métalliques «au trempé»), soit un composé minéral contenant les éléments du revêtement à réaliser. À ce dernier type appartient la catégorie des traitements de sulfuration ou de sulfonitruration en bain de sel. Ces bains contiennent des composés sulfurés (sulfates, thiosulfates) et des composés carburés ou carbonitrurés (carbonates, cyanures) qui se décomposent au contact du métal. Le revêtement obtenu est formé d’une superposition de couches minces de sulfures recouvrant le métal dont les zones superficielles sont nitrurées ou carbonitrurées. La cinétique de formation des couches est contrôlée par les vitesses de décomposition des composés du bain de traitement et par les vitesses de diffusion à l’état solide du soufre, du carbone et de l’azote, à la fois dans les couches formées et dans le métal sous-jacent.Parmi les traitements de dépôt métallique en bain fondu , les plus connus sont le zincage et l’étamage. Les traitements sont de courte durée (passage continu de la bande métallique dans le bain) à température assez modérée (260 0C pour l’étamage, 450 0C pour le zincage). L’état de surface du métal à revêtir (décapage, impuretés superficielles) est un paramètre important qui conditionne l’«accrochage» du revêtement par diffusion du métal protecteur dans les couches superficielles du métal à protéger.Un autre procédé de dépôt métallique consiste à projeter sur le métal de fines gouttelettes du revêtement en fusion (shoopage , métallisation au pistolet). Mais il est difficile dans ce cas d’invoquer l’intervention des phénomènes de diffusion pour expliquer l’adhérence des revêtements obtenus, puisque la température du métal de base reste voisine de l’ambiante.Parmi ces procédés de revêtement par diffusion à partir d’une phase liquide, citons aussi la métallisation par électrolyse en bain de sel fondu. C’est une électrolyse à haute température, en bain d’halogénures alcalins fondus, dans laquelle on utilise comme cathode le métal à protéger et comme anode le métal à déposer. Ce procédé cumule les avantages des dépôts électrolytiques (contrôle aisé des épaisseurs, contrôle de composition des bains...) et ceux des dépôts par diffusion (bonne adhérence des couches, formation de composés intermétalliques).Diffusion solide-solideLes phénomènes de diffusion entre deux phases solides sont mis à profit pour les traitements de surface dans trois cas principaux.Le plus simple est le placage , c’est-à-dire l’élaboration d’un revêtement protecteur par mise en contact du matériau de placage, acier inoxydable par exemple, et du substrat. L’adhérence par diffusion du placage est assurée par colaminage à haute température de l’ensemble métal + placage, suivi éventuellement d’un recuit de diffusion plus ou moins prolongé. Les lois mathématiques de la diffusion permettent de bien prévoir les profondeurs de la pénétration de l’un des métaux dans l’autre.Les mêmes lois s’appliquent lorsque, pour améliorer l’adhérence d’un dépôt métallique effectué à froid (par électrolyse par exemple), on est amené à effectuer un traitement thermique de diffusion. Le but est alors de remplacer l’interface métal-dépôt par une zone de diffusion plus ou moins étendue dont la résistance est bien meilleure.Enfin, un certain nombre de revêtements métalliques, comme le zincage ou le cadmiage, peuvent être effectués par mise en contact direct du métal de base avec une poudre du métal protecteur (sherardisation ). Dans ce cas d’ailleurs, il est probable que le métal déposé passe par la phase vapeur avant de diffuser dans le substrat, ce qui complique beaucoup la prévision des cinétiques d’élaboration du dépôt.3. Traitements de surface et propriétés mécaniquesLa tenue mécanique d’une surface est un paramètre très important non seulement lorsque la surface elle-même est soumise à des sollicitations mécaniques (frottement, usure), mais également si l’on considère que la plupart des ruptures (rupture fragile, rupture par fatigue, rupture par corrosion sous contrainte) trouvent leur origine dans des phénomènes superficiels.L’obtention de bonnes propriétés mécaniques superficielles est un domaine de choix de l’application des traitements de surface. Cependant, les exigences de l’utilisation du matériau sont bien souvent contradictoires:– une bonne résistance à l’usure est obtenue par un durcissement superficiel (par carburation, nitruration, trempe superficielle, «chromisation dure», etc.);– une bonne résistance à la propagation des fissures demande par contre une surface suffisamment plastique (dépôt de nickel par exemple) et, si possible, soumise à des contraintes de compression (écrouissage superficiel par grenaillage ou trempe superficielle...);– enfin, pour obtenir un frottement facile entre deux surfaces, il est bien souvent nécessaire d’avoir recours à des procédés de revêtement (sulfuration, placage...) qui confèrent à cette surface une plasticité suffisante sans diminuer de façon préjudiciable la résistance à l’usure [cf. FROTTEMENT].Parmi les traitements de surface mettant en œuvre d’importantes déformations superficielles, le plus répandu est sans doute l’usinage pur et simple. Il est en effet prouvé qu’un usinage, ou même un polissage mécanique, provoque la formation, aux environs de la surface, d’une zone dont la cristallisation est bouleversée par l’écrouissage, et ce sur une profondeur qui peut atteindre plusieurs dizaines, voire plusieurs centaines de micromètres (fig. 4). L’existence de cette zone écrouie est très bénéfique pour la tenue du matériau à l’usure et à la propagation des fissures. Son effet peut être encore amplifié par des traitements de grenaillage ou de billage.D’autres traitements mécaniques de surface, comme le sablage ou le microbillage, sont essentiellement utilisés pour la préparation de la surface en vue d’un traitement ultérieur. Le but à atteindre est, dans ce cas, d’augmenter la surface de réaction vraie par création d’une rugosité artificielle, et élimination des couches d’oxydes éventuelles.Le développement des traitements thermiques ou thermomécaniques de surface correspond au souci de disposer d’un matériau aussi ductile que possible dans sa masse et aussi dur que possible en surface, sans pour cela créer d’hétérogénéités importantes comme en provoquent les dépôts de revêtements. Un simple traitement thermique ou thermomécanique peut provoquer ce durcissement, par exemple par maintien de très courte durée à haute température de pièces en acier, suivi d’une trempe immédiate (recuit «flash»). De telles conditions sont obtenues par des chauffages à induction à haute fréquence («effet de peau»). Dans d’autres cas, il est possible de combiner le recuit superficiel avec un écrouissage localisé des zones proches de la surface par laminage à grande vitesse sans réduction de section («skin pass»).Le dernier facteur intervenant dans la tenue mécanique des surfaces est celui des contraintes résiduelles résultant d’un autre type de traitement. La plupart des dépôts sont en effet, au cours de l’élaboration elle-même, soumis à des contraintes dues par exemple aux phénomènes d’interdiffusion avec le métal sous-jacent ou inhérentes au procédé lui-même (gonflement des dépôts électrolytiques, contraintes dues au refroidissement brutal dans le shoopage). L’élimination de ces contraintes résiduelles, souvent néfastes, se fait, du moins partiellement, par un traitement thermique à température modérée.La très grande diversité des méthodes de traitement des surfaces rend délicat le choix d’un traitement donné dans un but déterminé. Les paramètres qui entrent en considération sont les mécanismes exacts de l’action de l’environnement sur le métal à traiter (diffusion, électrochimie, propriétés mécaniques et physiques), le but recherché par le traitement en fonction de ces mécanismes, la pondération entre les exigences souvent contradictoires de protection dans des environnements variables, les exigences du maintien d’un certain nombre de propriétés du matériau massif, les considérations économiques; il serait, par exemple, déraisonnable d’appliquer un revêtement coûteux pour protéger un matériau dont la durée de vie en fatigue, compte tenu des inclusions ou des microcriques inévitables, est inférieure à la durée de vie du revêtement choisi.
Le choix de la température de cémentation (850 à 1 000 0C) est lié à la grande solubilité du carbone dans l’austénite (2 p. 100 en poids), ce qui revient à dire que le couple de diffusion C/Fe 塚 devient une succession de couches C/Fe3C/austénite et que la forte solubilité du carbone dans l’austénite facilite la réaction de dissociation de la cémentite Fe3C à son interface avec l’austénite. La couche de cémentite est très mince, car la vitesse de diffusion du carbone y est très faible. Cette couche est généralement éliminée par un traitement postérieur dit «de diffusion». Par contre, la couche d’austénite chargée en carbone est épaisse (quelques millimètres). L’acier est ensuite trempé, ce qui transforme la couche cémentée en martensite de haute résistance mécanique. Les traitements de carburation en phase gazeuse sont appliqués pour la protection des métaux réfractaires oxydables (tungstène, molybdène) par une couche très dure de carbure.L’adjonction d’ammoniac à l’atmosphère de traitement, soit seul, soit en même temps que les composés carburants, constitue le procédé de nitruration ou de carbonitruration des aciers. Il se forme en surface une couche mince de nitrure Fe2N, recouvrant une zone profonde où le nitrure Fe4N est réparti en aiguilles dans la structure de l’acier. Ces couches améliorent dans de grandes proportions les propriétés mécaniques de surface des aciers et leur résistance à la corrosion.Les procédés de métallisation en atmosphères oxydoréductrices halogénées à l’équilibre (procédé Galmiche-O.N.E.R.A.) sont fondés sur le transport en phase vapeur de l’élément à déposer, à condition que celui-ci soit plus électropositif que le métal à protéger. En outre, il est nécessaire que les deux métaux possèdent un domaine de solubilité mutuelle à l’état solide. Il est ainsi possible de déposer du chrome sur le fer ou du fer sur le nickel, mais pas l’inverse. Le dépôt est obtenu en plaçant les pièces dans une enceinte sous pression d’hydrogène qui contient en outre une réserve d’halogénure métallique (fluorure, chlorure, etc.) volatil et les métaux d’apport sous forme finement divisée, associés éventuellement avec des constituants auxiliaires tels que des oxydes réfractaires. L’ensemble est porté à une température comprise entre 850 et 1 150 0C.Les équilibres d’oxydoréduction dans l’enceinte aboutissent à un transfert, par l’intermédiaire des halogénures volatils, du métal d’apport entre la poudre et la surface des pièces.Parmi les applications de ce procédé, une des plus répandues est la chromisation des aciers ou des matériaux réfractaires (à base de nickel, de cobalt, de molybdène, de tungstène). Dans le cas du fer ou des aciers par exemple, le traitement effectué à 950 0C environ (c’est-à-dire en phase 塚) aboutit à la formation en surface d’une couche de ferrite chargée en chrome (plus de 13 p. 100 de chrome), comme le montre le diagramme d’équilibre (fig. 2 a). Les grandes vitesses de diffusion du chrome en phase 見 à ces températures provoquent une croissance rapide de cette couche. Par contre, le chrome diffuse très lentement dans l’austénite sous-jacente qui est donc très peu modifiée (fig. 2 b). Après traitement, la surface est par conséquent recouverte d’une couche de quelques dizaines de micromètres d’acier riche en chrome, très résistante à la corrosion puisque passivable dans tous les milieux (fig. 3).Si l’acier a été au préalable carburé, le gainage correspond à une dispersion de carbure de chrome dans une matrice fer-chrome. L’épaisseur est plus faible en raison du blocage de la diffusion du chrome par une barrière de carbures. Par contre, la dureté superficielle est très élevée.Le traitement des superalliages réfractaires par ce procédé, en particulier en vue de leur application dans l’industrie aéronautique (turbines à gaz), met en œuvre un dépôt à partir d’un cément de poudres préalliées de chrome-aluminium («chromaluminisation»). Dans certains cas, les pièces sont prégainées par dépôt électrolytique de nickel ou de cobalt, ou par diffusion à partir d’un cément ternaire Ni-Cr-Ta («tancralisation»).Réactions solide-liquideUn autre type de traitement à température élevée consiste à mettre le métal en présence d’un milieu liquide qui peut être soit un métal en fusion (dépôts métalliques «au trempé»), soit un composé minéral contenant les éléments du revêtement à réaliser. À ce dernier type appartient la catégorie des traitements de sulfuration ou de sulfonitruration en bain de sel. Ces bains contiennent des composés sulfurés (sulfates, thiosulfates) et des composés carburés ou carbonitrurés (carbonates, cyanures) qui se décomposent au contact du métal. Le revêtement obtenu est formé d’une superposition de couches minces de sulfures recouvrant le métal dont les zones superficielles sont nitrurées ou carbonitrurées. La cinétique de formation des couches est contrôlée par les vitesses de décomposition des composés du bain de traitement et par les vitesses de diffusion à l’état solide du soufre, du carbone et de l’azote, à la fois dans les couches formées et dans le métal sous-jacent.Parmi les traitements de dépôt métallique en bain fondu , les plus connus sont le zincage et l’étamage. Les traitements sont de courte durée (passage continu de la bande métallique dans le bain) à température assez modérée (260 0C pour l’étamage, 450 0C pour le zincage). L’état de surface du métal à revêtir (décapage, impuretés superficielles) est un paramètre important qui conditionne l’«accrochage» du revêtement par diffusion du métal protecteur dans les couches superficielles du métal à protéger.Un autre procédé de dépôt métallique consiste à projeter sur le métal de fines gouttelettes du revêtement en fusion (shoopage , métallisation au pistolet). Mais il est difficile dans ce cas d’invoquer l’intervention des phénomènes de diffusion pour expliquer l’adhérence des revêtements obtenus, puisque la température du métal de base reste voisine de l’ambiante.Parmi ces procédés de revêtement par diffusion à partir d’une phase liquide, citons aussi la métallisation par électrolyse en bain de sel fondu. C’est une électrolyse à haute température, en bain d’halogénures alcalins fondus, dans laquelle on utilise comme cathode le métal à protéger et comme anode le métal à déposer. Ce procédé cumule les avantages des dépôts électrolytiques (contrôle aisé des épaisseurs, contrôle de composition des bains...) et ceux des dépôts par diffusion (bonne adhérence des couches, formation de composés intermétalliques).Diffusion solide-solideLes phénomènes de diffusion entre deux phases solides sont mis à profit pour les traitements de surface dans trois cas principaux.Le plus simple est le placage , c’est-à-dire l’élaboration d’un revêtement protecteur par mise en contact du matériau de placage, acier inoxydable par exemple, et du substrat. L’adhérence par diffusion du placage est assurée par colaminage à haute température de l’ensemble métal + placage, suivi éventuellement d’un recuit de diffusion plus ou moins prolongé. Les lois mathématiques de la diffusion permettent de bien prévoir les profondeurs de la pénétration de l’un des métaux dans l’autre.Les mêmes lois s’appliquent lorsque, pour améliorer l’adhérence d’un dépôt métallique effectué à froid (par électrolyse par exemple), on est amené à effectuer un traitement thermique de diffusion. Le but est alors de remplacer l’interface métal-dépôt par une zone de diffusion plus ou moins étendue dont la résistance est bien meilleure.Enfin, un certain nombre de revêtements métalliques, comme le zincage ou le cadmiage, peuvent être effectués par mise en contact direct du métal de base avec une poudre du métal protecteur (sherardisation ). Dans ce cas d’ailleurs, il est probable que le métal déposé passe par la phase vapeur avant de diffuser dans le substrat, ce qui complique beaucoup la prévision des cinétiques d’élaboration du dépôt.3. Traitements de surface et propriétés mécaniquesLa tenue mécanique d’une surface est un paramètre très important non seulement lorsque la surface elle-même est soumise à des sollicitations mécaniques (frottement, usure), mais également si l’on considère que la plupart des ruptures (rupture fragile, rupture par fatigue, rupture par corrosion sous contrainte) trouvent leur origine dans des phénomènes superficiels.L’obtention de bonnes propriétés mécaniques superficielles est un domaine de choix de l’application des traitements de surface. Cependant, les exigences de l’utilisation du matériau sont bien souvent contradictoires:– une bonne résistance à l’usure est obtenue par un durcissement superficiel (par carburation, nitruration, trempe superficielle, «chromisation dure», etc.);– une bonne résistance à la propagation des fissures demande par contre une surface suffisamment plastique (dépôt de nickel par exemple) et, si possible, soumise à des contraintes de compression (écrouissage superficiel par grenaillage ou trempe superficielle...);– enfin, pour obtenir un frottement facile entre deux surfaces, il est bien souvent nécessaire d’avoir recours à des procédés de revêtement (sulfuration, placage...) qui confèrent à cette surface une plasticité suffisante sans diminuer de façon préjudiciable la résistance à l’usure [cf. FROTTEMENT].Parmi les traitements de surface mettant en œuvre d’importantes déformations superficielles, le plus répandu est sans doute l’usinage pur et simple. Il est en effet prouvé qu’un usinage, ou même un polissage mécanique, provoque la formation, aux environs de la surface, d’une zone dont la cristallisation est bouleversée par l’écrouissage, et ce sur une profondeur qui peut atteindre plusieurs dizaines, voire plusieurs centaines de micromètres (fig. 4). L’existence de cette zone écrouie est très bénéfique pour la tenue du matériau à l’usure et à la propagation des fissures. Son effet peut être encore amplifié par des traitements de grenaillage ou de billage.D’autres traitements mécaniques de surface, comme le sablage ou le microbillage, sont essentiellement utilisés pour la préparation de la surface en vue d’un traitement ultérieur. Le but à atteindre est, dans ce cas, d’augmenter la surface de réaction vraie par création d’une rugosité artificielle, et élimination des couches d’oxydes éventuelles.Le développement des traitements thermiques ou thermomécaniques de surface correspond au souci de disposer d’un matériau aussi ductile que possible dans sa masse et aussi dur que possible en surface, sans pour cela créer d’hétérogénéités importantes comme en provoquent les dépôts de revêtements. Un simple traitement thermique ou thermomécanique peut provoquer ce durcissement, par exemple par maintien de très courte durée à haute température de pièces en acier, suivi d’une trempe immédiate (recuit «flash»). De telles conditions sont obtenues par des chauffages à induction à haute fréquence («effet de peau»). Dans d’autres cas, il est possible de combiner le recuit superficiel avec un écrouissage localisé des zones proches de la surface par laminage à grande vitesse sans réduction de section («skin pass»).Le dernier facteur intervenant dans la tenue mécanique des surfaces est celui des contraintes résiduelles résultant d’un autre type de traitement. La plupart des dépôts sont en effet, au cours de l’élaboration elle-même, soumis à des contraintes dues par exemple aux phénomènes d’interdiffusion avec le métal sous-jacent ou inhérentes au procédé lui-même (gonflement des dépôts électrolytiques, contraintes dues au refroidissement brutal dans le shoopage). L’élimination de ces contraintes résiduelles, souvent néfastes, se fait, du moins partiellement, par un traitement thermique à température modérée.La très grande diversité des méthodes de traitement des surfaces rend délicat le choix d’un traitement donné dans un but déterminé. Les paramètres qui entrent en considération sont les mécanismes exacts de l’action de l’environnement sur le métal à traiter (diffusion, électrochimie, propriétés mécaniques et physiques), le but recherché par le traitement en fonction de ces mécanismes, la pondération entre les exigences souvent contradictoires de protection dans des environnements variables, les exigences du maintien d’un certain nombre de propriétés du matériau massif, les considérations économiques; il serait, par exemple, déraisonnable d’appliquer un revêtement coûteux pour protéger un matériau dont la durée de vie en fatigue, compte tenu des inclusions ou des microcriques inévitables, est inférieure à la durée de vie du revêtement choisi.
Encyclopédie Universelle. 2012.
